Die Süddeutsche Zeitung ist weder für den Inhalt der Anzeige noch die darin enthaltenen Verlinkungen noch für ggf. angegebene Produkte verantwortlich.
Pressemitteilungen auf SZ.de
Lesen Sie hier aktuelle Pressemitteilungen im Presseportal der Süddeutschen Zeitung. Unser Partner news aktuell GmbH (ein Unternehmen der dpa-Gruppe) stellt Ihnen Presseerklärungen, Pressemeldungen und -informationen zu Ereignissen, Produkten und Veranstaltungen verschiedenster Unternehmen zur Verfügung.
Die Meldungen nach Veröffentlichungszeitpunkt
EDEKA ZENTRALE Stiftung & Co. KG
25.04.2024 - 13:00
Geschäftsjahr 2023: EDEKA-Verbund wächst in einem schwierigen Marktumfeld
webfleet
25.04.2024 - 11:00
Neues Webfleet-Tool unterstützt Nutzfahrzeugflotten beim datengesteuerten Umstieg in die Elektromobilität
Leon Migge
25.04.2024 - 08:17
Traum-Abitur: Wie Leon Migge Oberstufenschülern mit stressfreiem Lernen zu besseren Noten und mehr Freizeit verhilft
Pfizer Pharma GmbH
24.04.2024 - 16:41
Aktuelle Umfrage zeigt: Deutsche lassen ihr Auto häufiger überprüfen als ihre Gesundheit
GlaxoSmithKline GmbH & Co. KG
24.04.2024 - 13:19
Welt-Impfwoche 2024 / Umfassender Meningokokken-Schutz kann lebenslange Folgen bei Babys und Kleinkindern verhindern
m2c - medical concepts & consulting
24.04.2024 - 13:04
Full-Service-Agentur m2c: Praxismarketing für Zahnärzte
UHRIG Handelsgesellschaft mbH
24.04.2024 - 10:38
Retourenhandel als Geschäftsmodell: Wie Manuel Uhrig von der UHRIG Handelsgesellschaft mbH die Händler auf Wachstumskurs bringt
WHITEBLICK DR FEISE + KOLLEGEN
23.04.2024 - 16:54
Feste Zähne an einem Tag - in der Zahnarztpraxis WHITEBLICK in Stuttgart
HARTING Stiftung & Co. KG
23.04.2024 - 16:02
Bundeskanzler besucht HARTING auf der HANNOVER MESSE / Technologiegruppe präsentiert Innovationen für eine klimaneutrale Zukunft
BUND
23.04.2024 - 10:30
BUND und BDEW: PFAS-Belastung - Hersteller sollen zahlen / BUND findet Ewigkeits-Chemikalien in Mineral- und Leitungswasser
Ford-Werke GmbH
23.04.2024 - 10:00
Schneller laden und weiter fahren: Ford Pro wertet den vollelektrischen Marktführer E-Transit weiter auf
dpa Deutsche Presse-Agentur GmbH
23.04.2024 - 10:00
Faktencheck24: dpa bietet in Kooperation mit der Google News Initiative Journalismus-Trainings rund um Social Media und KI an
Lets GmbH
22.04.2024 - 11:25
Gemeinsam für mehr soziales Engagement: TSV 1860 München, die Bayerische Versicherung und Lets GmbH organisieren gemeinsames Clean-Up-Projekt an der Isar
APEX Consulting
22.04.2024 - 10:01
Jousef Murad von APEX Consulting klärt auf: Google's Search Generative Engine (SGE) wird Ihr Marketing verändern!
World Vapers' Alliance
22.04.2024 - 06:05
Großbritanniens umstrittene Rauchverbotspläne: ein risikoreicher Kurswechsel
L'Oréal Paris
19.04.2024 - 15:47
Neue Studienergebnisse von L'Oréal Paris in Zusammenarbeit mit IPSOS identifizieren Belästigung in der Öffentlichkeit als Auslöser zunehmender Unsichtbarkeit von Frauen in der Gesellschaft
Tourismusverband Mondsee-Irrsee
19.04.2024 - 12:29
Lauf- und Radsportkalender 2024 - im Mondseeland ist was los
Hotel FAYN garden retreat ****superior
19.04.2024 - 12:20
Mehr Glanz und Luxus im 4 Sterne Superior Hotel Fayn in Südtirol
Arbeitsbühnen Seeger GmbH
18.04.2024 - 17:05
Ob Spezialarbeitsbühne oder Teleskopstapler: zuverlässig mieten bei der Arbeitsbühnen Seeger GmbH
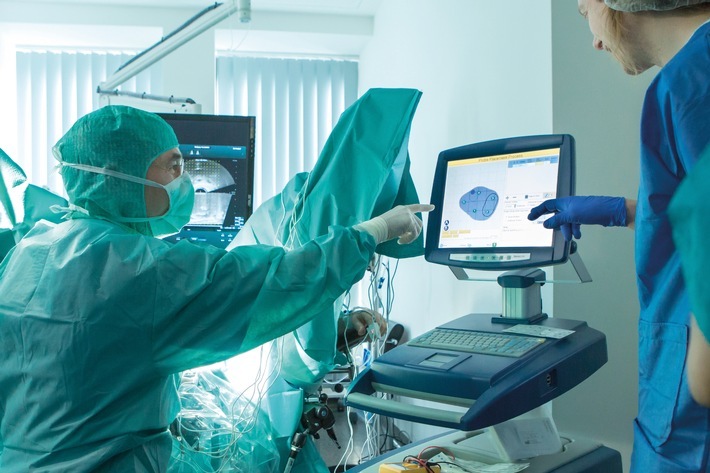
VITUS Privatklinik Prof. Dr. Stehling GmbH
18.04.2024 - 16:44
Weltweit führender Experte für fokale Prostatakrebstherapie an der VITUS Privatklinik in Offenbach
MTEL Deutschland GmbH
18.04.2024 - 16:17




.jpg?crop=0,0,800,600)







%20(1).jpg?crop=0,0,800,600)
.jpg?crop=0,0,800,600)